2022/12/26
1剤で売上1兆円超えも。イチからわかる「医薬品ビジネス」
NewsPicks Brand Design シニアエディター
コロナパンデミックの襲来で医薬品の重要性を誰もが痛感したこの2年。
世界の医薬品市場は拡大の一途を辿り、2024年には160兆円規模に達すると予測されています。
従来、スイスや米国などのメガファーマ(巨大製薬企業)が潤沢な研究開発費を背景に新薬を生み出し市場を牽引してきましたが、近年では創薬のニーズの変化に伴い、製薬企業のビジネスモデルも変化しつつあります。
そんな医薬品市場の動向について、ビジネスパーソンなら知っておきたいトピックを専門家がQ&A形式で解説します。
※当記事は素材メーカーAGCのスポンサードコンテンツです。本文では同社のCDMO(医薬品等の開発製造受託機関)事業の取り組みも紹介します

東京工業大学大学院理工学研究科(修士)卒業後、国内製薬企業で合成創薬研究に携わる。2007年に退職し、フリーのサイエンスライターに転身。2009年より2012年まで、東京大学大学院理学系研究科化学専攻にて広報担当特任助教。主な著書に「医薬品クライシス」(新潮新書)、「創薬科学入門」(オーム社)、「世界史を変えた薬」(講談社現代新書)など。
……医薬品は大きく2種類に分かれる?
病気になると、誰もがお世話になる医薬品。一口に薬といっても、実は大きく2種類に分かれます。
医療機関を受診した後、処方箋をもらって薬局で買うのが「医療用医薬品」、処方箋なしで買えるのが「一般用医薬品」です。
一般に、強い効果があり、医師の診断に従った使用が必要な薬が前者に、効き目がマイルドで、一般の人が自分の判断で使用でき、ドラッグストアなどで入手しやすい薬が後者にカテゴライズされています。
両者は流通経路も価格設定方法も異なり、商品としては全くの別物です。
また、市場規模にも大きな差があり、医療用医薬品の国内市場が約10兆円に上るのに対し、一般用医薬品は8000億円前後にすぎません。
okskaz / istock
新しい医療用医薬品を一つ創り出すには、10年以上の歳月と数百億円の費用がかかるケースが多いことから、医療用医薬品メーカーには十分な資金力と組織体制が必要です。
このためCMを多く流す一般用医薬品メーカーより知名度は低いものの、企業規模では遥かに上、という会社も少なくありません。
この記事では、医療用医薬品の世界にスポットを当て、その特徴を紹介していきます。
製薬企業には、大きく二つのビジネスモデルがあります。
一つは先発医薬品メーカーと呼ばれるタイプ。多大な研究開発費を投じて新薬を創出し、特許期間中に独占販売することで利益を生み出します。
中には、1剤で1兆円を超える莫大な売上を計上することもあります(※)。
※2021年に世界で最も売れた医薬品と言われる米アッヴィ社の関節リウマチ治療薬「ヒュミラ」は、昨年だけで4兆円を超える売上を記録している
もう一つは後発医薬品メーカーと呼ばれる製薬会社です。
先発医薬品メーカーが開発した新薬の特許が切れた後に、同じ成分の安価な薬(ジェネリック医薬品)を発売し、利益を出すビジネスモデルです。
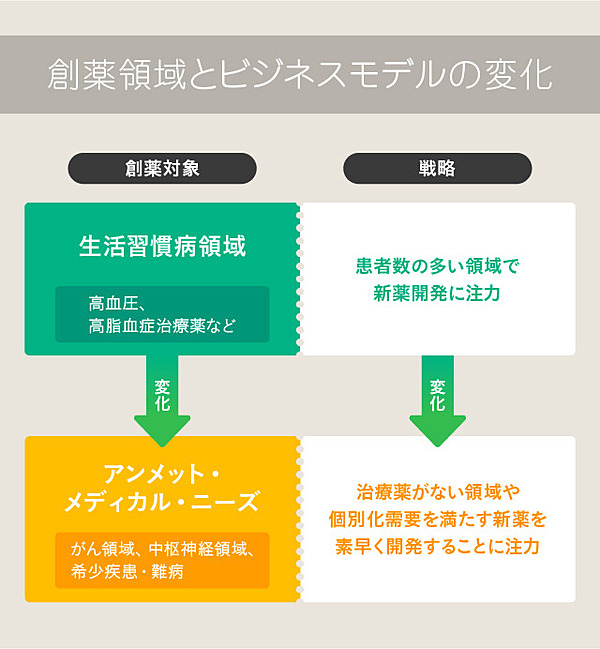
2000年代まで、世界の先発医薬品メーカーは高血圧や高脂血症といった、生活習慣病の治療薬を主力製品としていました。
これらは、化学合成の技術で作られたものが主体でした。
一方で、1990年代頃からの遺伝子組み換え技術の急速な進展に伴い、一部の製薬会社やバイオベンチャーは「バイオ医薬品」と呼ばれる新しいタイプの医薬品の研究開発に取り組み始めました。
その後、抗体の利用などの技術革新により、従来型の技術では十分な治療薬が存在していなかったがんやリウマチなどの難病、すなわちアンメットメディカルニーズ(※)にも効果が確認されると、バイオ医薬品がより脚光を浴びるようになりました。
多くの製薬会社・バイオベンチャーが相次いで参入し、バイオ医薬品の市場が大きく拓かれていったのです。
※まだ満たされていない医療上のニーズ。製薬業界では創薬需要の高い領域と見なされている
バイオ医薬品は、生体内で働くホルモンや抗体などの構造を一部改変し、医薬品として用いるものです。
その開発・製造には、遺伝子組換え技術などのバイオテクノロジーが主役となります。
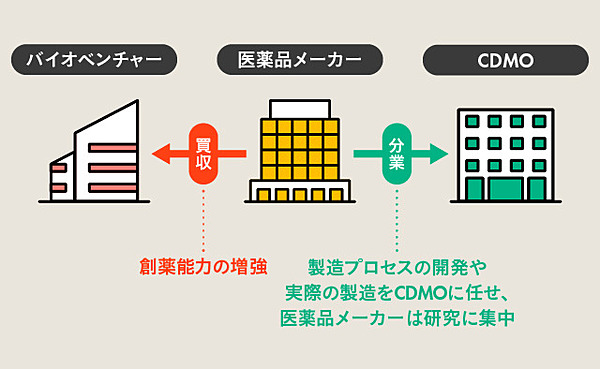
旧来の医薬品とは全く異なるノウハウや、培養槽など新たな大型設備の導入が不可欠になることから、大企業によるバイオベンチャーへの出資が盛んになり、会社ごと買収してそのノウハウを吸収することも活発に行われています。
こうした動きにつれて、製薬業界の構造も大きく変化しました。
かつての製薬企業は、研究開発から製造・販売までを一社で全て行うことが普通でした。
しかしバイオ医薬品をはじめとしたより構造が複雑な医薬品へのシフトのために、資金を研究段階に集中させる必要が生じてきたのです。
このため製薬企業が、研究段階ではバイオベンチャーと、臨床試験や製造段階ではCDMO(医薬品等の開発製造受託機関)と連携する、水平分業化が進行しています。
以上の背景から、近年では先進的なバイオベンチャーが脚光を浴びるほか、高い専門技術を持ったCDMOの存在感が急速に高まっています。
バイオ医薬品は、バイオテクノロジーを用いて製造される医薬品を指す言葉であり、かなり幅広い医薬品が含まれます。
前述した抗体やホルモンをもとにしたもののほか、各種のワクチンや、DNA・RNAなど核酸類を用いるもの、細胞やウイルスを用いる治療薬も、バイオ医薬品に含まれます。
錠剤やカプセルなど、我々が「医薬品」といって思い浮かべる姿からはずいぶんかけ離れたものも、今や医薬品の範疇なのです。
中でも、抗体(人間の免疫作用の一端を担う体内物質)を利用した「抗体医薬品」は、バイオ医薬品のエース格ともいえる存在であり、今まで難しかったがんやリウマチなどの治療に新しい道を開きました。
本庶佑氏にノーベル賞をもたらしたがん治療薬「オプジーボ」も、抗体医薬品の一種です。
バイオ医薬品は一般に副作用が少なく、疾患のタイプに合わせたきめ細かい医療が可能になるという特徴も併せ持ちます。
このため、多くの製薬企業がバイオ医薬品の開発に力を入れるようになりました。
近年では、世界医薬品売上トップ10の6、7製品までが、バイオ医薬品で占められるようになっています。
また、新型コロナや認知症の治療薬にも応用が図られるなど、その活躍の場はさらに広がりつつあります。
“グローバルCDMO”としての存在感を高めるAGC
医薬品が世に出るまでには、研究・臨床試験・製造などの段階を踏む必要がある。研究段階では、「医薬品の種」となる候補物質を創出する。
臨床試験では、試験用の医薬品を少量生産し、実際の患者を対象とした試験を行い、候補物質の効能や安全性などを調べる。
製造段階では、量産化に向けた製造プロセスを開発し、また、高品質な医薬品の安定的な製造体制を構築しなければならない。
前述のように、製薬業界ではこれらの段階を別々の会社で行う、水平分業化が進んでいる。
多様かつ複雑な構造を持つ医薬品が登場し、移り変わりも早い現在では、全てを自社内で行うよりも分業が合理的といえる。
こうした中で、「CDMO」と呼ばれる存在がクローズアップされている。
CDMOは、医薬品等の開発製造受託機関(Contract Development and Manufacturing Organization)の略称で、臨床試験に用いる治験薬から実際の医薬品まで、その製造プロセスの開発や製造などを受託する企業を指す。
医薬品は、患者の体内に入り、直接生命のシステムにタッチする製品であるため、極めて高い品質が求められる。健康の維持に不可欠であることから、品切れなども許されない。
このため医薬品製造にはGMP(Good Manufacturing Practice=医薬品及び医薬部外品の製造管理及び品質管理の基準)と呼ばれる厳密な規定があり、製造体制などについて厳しい審査を経る必要がある。CDMOも、当然こうした基準を満たさねばならない。
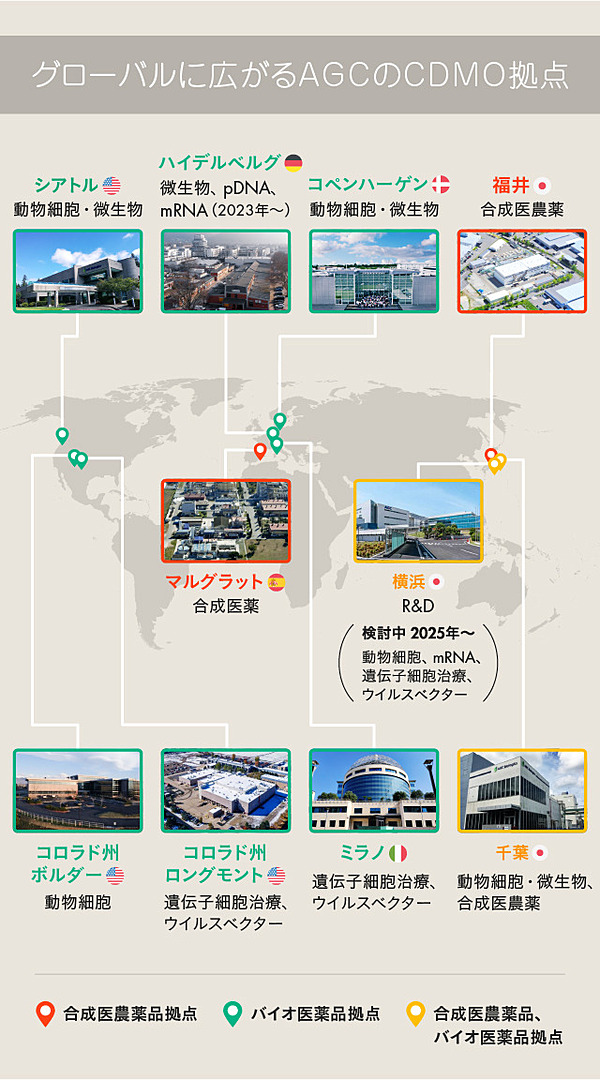
AGCは、日本に本拠を置く数少ないグローバルなCDMOだ。
先進的な技術を有する海外企業のM&Aや設備投資を連続的に実行し、その拠点は日米欧の10カ所まで広がりをみせる。
化学合成による医薬品・農薬はもちろん、微生物や動物細胞を用いたバイオ医薬品、さらに遺伝子・細胞治療薬といった先端的な医療までも幅広くカバーする体制を築き上げている。
同社は25年以上にわたってCDMOとしての実績を積み上げた。
顧客から高い信頼を獲得し、近年では高いレベルの管理体制を必要とする開発後期や販売用の案件の受注が増加、今後も事業拡大が見込まれているという。
シアトル、ミラノ、横浜のR&Dセンターを軸にグローバルに統合された高水準の生産体制を築き上げたAGCは、業界きってのCDMOとして、ビジネスモデルが大きく変わりつつある医薬品産業において、大きな存在感を示している。
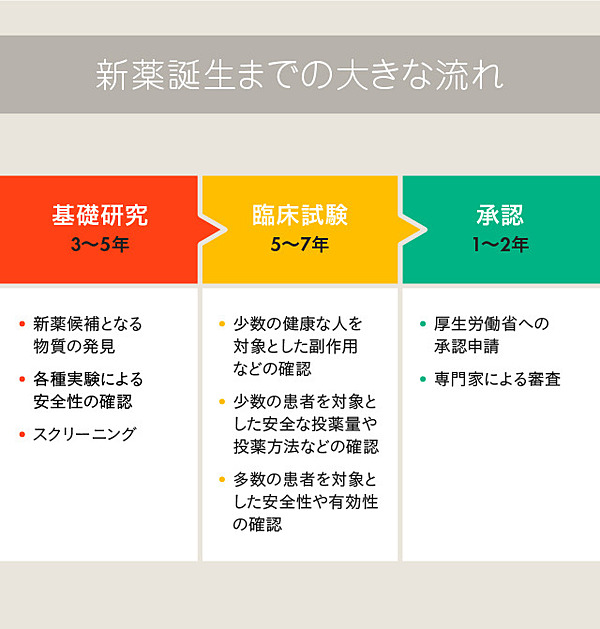
多くの場合、医薬品が承認を受けて市場に出るまで、10年以上の時間がかかります。
まず、医薬品候補となる物質を探す研究段階においては、各種の実験のデータを見ながら候補物質を改良し、より効果と安全性が高いものを選び出していきます。この段階には、3~5年の時間を要します。
こうして選び出された化合物は、臨床試験で実際の患者に投与され、人体にも効果があるかどうか調べられます。少しずつ被験者を増やし、段階を踏みながら薬効と安全性を調べていきます。
慎重かつ精密に試験を進めねばならないため、臨床試験は通常5年から7年、場合によっては10年程度の歳月を要します。製薬企業にとっては、最も時間や資金がかかる段階です。
この一連の臨床試験においても水平分業が広がり、製剤設計や治験薬製造など、CDMO事業者が担う役割も大きくなっています。
こうして臨床試験で得られたデータは、国の機関によって厳密な審査を受けます。
不正行為がないよう、失敗した実験データを含めて全てを提出する必要があり、その書類だけでトラック1台分になると言われるほど、膨大なものになります。
審査段階では、これらのデータに漏れや改ざん、記載ミスなどがないか、統計処理やデータの解釈に不備はないか、専門的な見地からの審議が行われます。
このため、審査にも1~2年ほどの時間を要します。
このように、安全で有効な医薬品を創り出すためには、どうしても10年前後の歳月がかかってしまうのです。
一方で、一刻も早い新薬の登場を待ち望む患者さんが多くいることも事実です。迅速な新薬創出への努力は、今も続けられています。
今をときめくバイオ医薬品の多くは、タンパク質を本体としています。
タンパク質は体内で様々な生理作用を担う重要な物質群であり、利用の仕方次第で優れた医薬品となりうるのです。
ただし、タンパク質の製造はコストがかかり、保管などにも気を使う必要があります。
そこで、タンパク質の設計図であるメッセンジャーRNA(mRNA)を体内に送り込み、人体のタンパク質合成システムを使って必要なタンパク質を作らせるアイディアが生まれました。
これをやってのけたのがモデルナ社やファイザー社の新型コロナワクチンで、世界のコロナ禍抑制に大きな貢献を果たしました。
また、mRNAを用いて、ワクチンだけでなく治療用として機能するタンパク質を体内で作らせることも可能です。
これらはmRNA医薬品と呼ばれ、ワクチン用途ではインフルエンザなど各種感染症のワクチンへの展開、治療用途ではがん治療や再生医療などへの応用が期待されています。
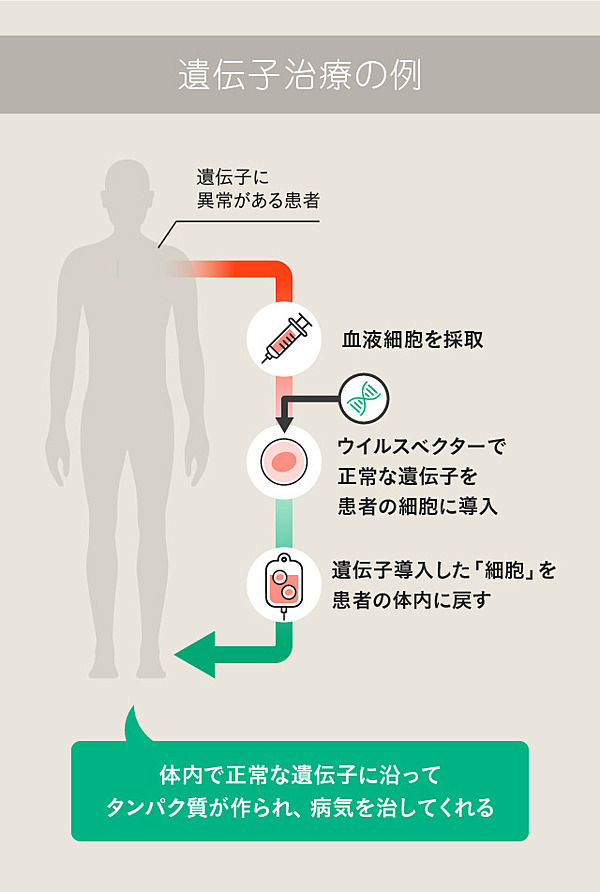
また、遺伝子または遺伝子を導入した細胞を体内に投与する治療法(遺伝子・細胞治療)も大きく進展しています。
患者自身の体から取り出した免疫細胞に対して、ウイルスベクター(※)等を用いて遺伝子を導入し、がん細胞と戦う能力を付与した上で、体内に戻してがんを治療するという方法が、その一例です。
※細胞内に望みの遺伝子を導入するウイルス由来の運搬体。ウイルスが細胞に入り込む性質を利用する。
この方法はCAR-T療法と呼ばれ、難治性のがん治療に実績を上げつつあります。
今までの常識では、とても「医薬品」とは呼べないような治療法ですが、これが「新薬」として承認を受け、薬価がつけられる時代に入っているのです。
新たなタイプの医薬としては、他にも多くの可能性が考えられています。
中でもCAR-T療法に代表されるように、一人ひとりの疾患の性質に合わせた治療を目指す、個別化医療の方向が大きなトレンドといえるでしょう。
国内のバイオ医薬品製造増強へ。期待集めるAGCの新設備
コロナ禍において、国産ワクチンの創出が成らず、国民の生命を守るワクチンを外国企業に委ねざるを得なかったことは、我々にとって大きな衝撃であった。
パンデミック発生時にワクチンが素早く用意できるかどうかは、国家の安全保障そのものであるということが、改めて認識されたのだ。
そこで経済産業省は、次なるパンデミックに備え、ワクチン製造体制の強化に乗り出している。
AGCはこの事業(※)に採択され、横浜テクニカルセンター(YTC)を拠点としたバイオ医薬品CDMO事業の能力拡大に向けた検討を進めている。
※経済産業省「ワクチン生産体制強化のためのバイオ医薬品製造拠点等整備事業」
AGCの国内拠点としては、千葉工場に次ぐ第二のバイオ医薬品開発・製造拠点となる。
注目されるのは、平時にはバイオ医薬品を製造し、パンデミックの際にはワクチン製造に切り替えができる「デュアルユース」設備の導入だ。
組み換えタンパク質ワクチン、mRNAワクチン、ウイルスベクターワクチン、遺伝子改変細胞ワクチンなど、多くのタイプのワクチン製造に対応できる設備を整えることで、現在想定されるほとんどのタイプのワクチンを製造する能力を手に入れることになる。

AGC横浜テクニカルセンター
AGCがこの事業に採択された理由は、その確かな実績にある。
すでに同社は千葉工場において、日本や欧米各社のバイオ医薬品製造を委託されており、高い評価を受けていた。
コロナ禍においても、世界各社のワクチン・治療薬候補の製造を数多く手がけるなど、大きな貢献を積み重ねてきた。
横浜拠点にも、1万~2万Lという国内最大級の動物細胞のバイオリアクターを導入する予定としている。
これが稼働すれば、現在のところ海外依存度の高いバイオ医薬品を、国内で開発・製造する能力が大きく向上する。
AGCは基盤となっている医薬品・農薬のCDMOサービスの更なる能力強化を進める一方で、サービス・事業領域の拡大も着々と進めている。
先端分野である遺伝子・細胞治療薬についてすでに取り組みを開始している中、mRNA医薬品についても2023年にはサービス提供体制を整える。
加えて、再生医療や開発黎明期にあるその他の新技術についても、参入を検討しているという。
高度な技術が生み出してきた実績と信頼。先を見つめる確かな目。多様な強みを武器に、AGCは医薬品業界の発展を推し進めている。
執筆:佐藤健太郎
撮影:北山宏一
デザイン:久須美はるな
編集:下元陽