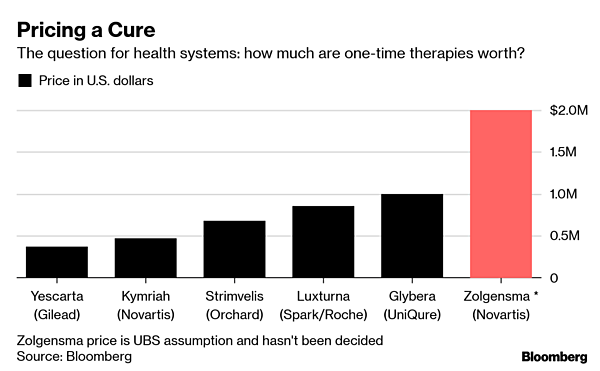
ノバルティスは分割払いを検討
欠陥のあるDNAを修復し、致死性の小児疾患や珍しい血液疾患などの重病を治療する革命的な遺伝子治療の開発ラッシュが起きている。
しかし、こうした未来の治療法に対する興奮の下には、重要な問題が隠されている。治療にいくらかかるかを知っている人がいないという問題だ。
これらの新しい治療法は、1回の治療で病気の根本原因を取り除くことを目標としている。具体的には、正常な遺伝物質を患者の細胞に導入するという方法がとられる。この治療を受けることで高価な薬を一生使い続けなくて済むのであれば、たとえ治療費が数百万ドルでも、治療にかかる総額は大幅に減る可能性がある。
スイスの製薬大手ノバルティスのバス・ナラシンハンCEOは「世界の医療保険業者のほとんどはこのような経験がない。とくに、これらの治療法の多くが現実になったら、彼らは新しいモデルをつくらなければならないだろう」と述べる。「われわれは適応可能なシステムを必要としている」
ノバルティスは1つの答えとして、分割払いを導入し、初期費用を減らすことを提案している。実際、進行性の筋肉疾患を対象とする、認可間近の治療法「Zolgensma」では分割払いの導入を計画している。
遺伝子治療は患者と会社の利益に大きな影響をもたらすと考える製薬会社は増えている。
ファイザーは3月、パリに本社を置くヴィヴェ・セラピューティクス(Vivet Therapeutics)と手を組み、珍しい肝臓疾患の治療法を開発することで合意した。米食品医薬品局(FDA)は2025年までに、毎年20もの細胞治療や遺伝子治療を認可することになると予測している。
ただし、これらの治療法が劇的な結果をもたらすかどうかについては懐疑的な見方も多く、価値の判断が難しくなっている。
ボストンに本拠を置くNPO「臨床経済的評価研究所(ICER)」のスティーブン・ピアソン所長は、画期的な治療法を切実に求めている患者に届けるためには、合理的な価格設定が不可欠だと指摘する。
薬価設定に関するICERのレポートは、アメリカの医薬品支出を巡る議論に影響を与えている。価格が低すぎれば、投資の妨げになる一方で、法外な価格は国の医療ネットワークの負担になる。
ピアソン所長はあるインタビューで「患者に価値をもたらすことが考えられていないように見える、法外な価格は問題だ。貨物列車が猛スピードでレンガの壁に激突するようなことがないシステムを、作り出す必要がある」と述べている。そうしたことを守らなければ、「おそらくシステムは凍り付いてしまうだろう」
治療費が数百万ドルに上る可能性も
ノバルティスのZolgensmaは、まだ始まったばかりのこの分野のテストケースだ。
脊髄性筋萎縮症(SMA)の治療法であるZolgensmaは、アメリカで規制当局の判断を待っているところだが、UBSグループのアナリストは約200万ドルの価格設定になると予測している。もしそうなれば、アメリカ初の200万ドルを超える治療法となる。
ICERは2月のレポートで、Zolgensmaの価値は最大150万ドル、最小31万ドルという試算を発表した。一方、ノバルティスは別の分析法を用い、Zolgensmaの価値は最大500万ドルという数字を導き出している。
ICERは、4月に入ってから最終的なレポートを発表。その際、Zolgensmaの価値は「メーカーが正当と主張した400万~500万ドルよりはるかに低いはずだ」と述べている。
Zolgensmaの代わりとなる治療法は、現行の治療法であるバイオジェンの「スピンラザ」で、こちらは生涯にわたって投与しなければならない。バイオジェンは、アメリカで2年前に発売されたスピンラザについて、Zolgensmaよりエビデンスが多いと述べている。
ノバルティスはこれに対し、Zolgensmaも5年分に近いデータがあると反論している。スピンラザの治療費は10年間で約410万ドルだ。
ナラシンハンCEOによれば、ノバルティスは5年間の分割払いを計画しているという。また、5年以内に患者が死亡するか治療が失敗に終わった場合は、払い戻しが行われる。
「われわれは、5年間だけ支払いを求め、その後、支払いはゼロになる」とナラシンハンCEOは話す。「治療によって子どもたちが生き続けられる価値を考えてみてほしい。非常に大きな価値がある」
分割払いを検討している企業はほかにも多数ある。ブルーバード・バイオは同社初となる遺伝子治療について、コストの最大80%が数年間の実績によって変化する可能性があると述べている。価格は最大210万ドルに設定されている。
ブルーバードのニック・レシュリーCEOは「われわれは一生ものとしての価値があると信じているが、リスクを共有しなければならないとも考えている。なぜなら、真っすぐ目を見て(長期的な効果を)100%約束すると言うことができないためだ」と話す。
「治療の成功」をどう定義すべきか
高額の遺伝子治療が大当たりした例はまだない。免疫系疾患の治療法で、約67万5000ドルかかるグラクソ・スミスクラインの「Strimvelis」は、少数の患者に使われただけで、オーチャード・セラピューティクスに売却された。
こちらも珍しい疾患の治療法で、100万ドルかかるユニキュア(UniQure)の「Glybera」も、すでに販売を終了している。ノバルティスの「Kymriah」など、患者の免疫細胞を変化させてガンと闘う治療法も苦戦している。
今後とくに注目されると見られるのは、血友病の治療法だ。スパーク・セラピューティクスなどが開発しており、同社は2月、ロシュ・ホールディングに買収されることが決まった。血友病は血液凝固因子の異常を伴う疾患で、生涯の治療費は数千万ドルに上る。遺伝子治療の価格も、この金額を反映したものになるだろう。
英国政府に対して医薬品支出の助言を行う、英国立医療技術評価機構の科学ディレクター、ニック・クラブは「これらの治療法が、極めて珍しい疾患だけでなく、患者の多い疾患にも用いられるようになれば、数百万ドルの価格はいずれ持続不可能になるだろう」と述べる。「そのことを理解するのが重要だ」
英国とカナダでは、遺伝子治療の到来に備え、医薬品の価格を決定する当局がICERと連携し、有望な治療法の新しい評価方法をテストしている。
ボストンに拠点を置く医療保険「ハーバード・ピルグリム・ヘルスケア」の最高医療責任者マイケル・シャーマンは、治療の成功について双方がどのように定義するか、長期的なエビデンスの不足をどう説明するかなどが障害になると予想している。
価格そのものが高すぎれば、分割払いを提供しても、ジレンマの解決にはならないだろう。スタート地点が公正でなければ、「高すぎる薬の支払いを楽にするためだけに、分割払いすることになるかもしれない」
(執筆:James Paton記者、翻訳:米井香織/ガリレオ、写真:©2019 Bloomberg L.P)
©2019 Bloomberg L.P
This article was translated and edited by NewsPicks in conjunction with IBM.